對抗鐮刀型紅血球病 FDA批准首件基因療法CRISPR
編譯/高晟鈞
美國食品藥物管理局週五批准了兩種治療鐮刀型紅血球疾病的基因療法,其中之一便是第一個在美國獲得監管批准的基因療法──CRISPR/Cas9。
這項消息將是鐮刀狀細胞治療的一大里程碑。「鐮刀型細胞疾病是一種罕見、且危及生命的血液疾病。我們很高興通過批准兩種基因療法來推動該領域,特別是對於生活受到該疾病嚴重困擾的患者而言。」FDA生物製品評估與治療產品辦公室主任Nicole Verdum在聲明中說道。
更多新聞:英國獲批CRISPR基因編輯療法 打開治療遺傳疾病大門
鐮刀型紅血球疾病
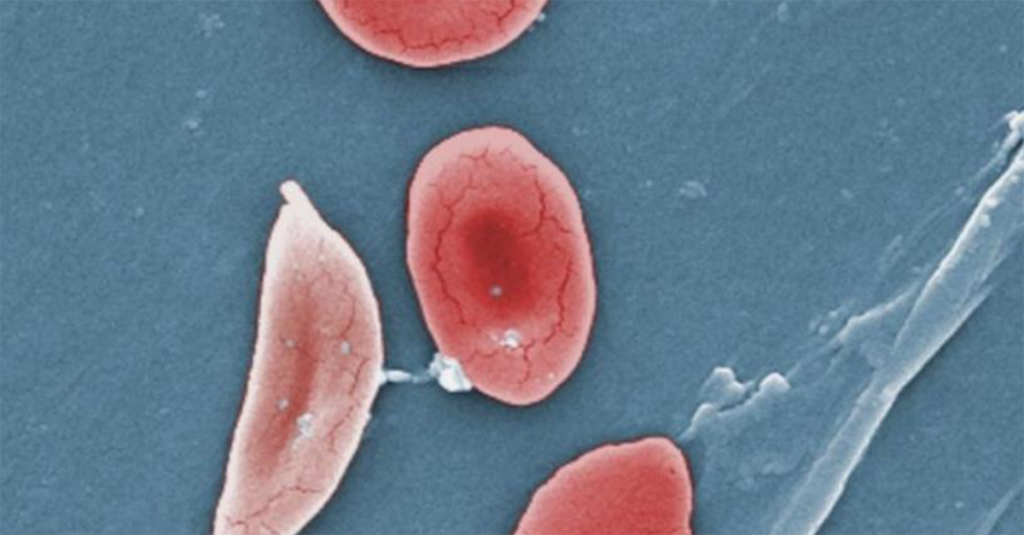
鐮刀型紅血球疾病是一種毀滅性的遺傳疾病,紅血球會變形為鐮刀狀並堵塞血管。在美國,鐮刀狀疾病影響超過10萬人,其中最常見的是非裔美國人。它會導致貧血、血管阻塞、中風和不可逆的器官損傷,甚至造成死亡。
直到今天,該疾病的治療依舊有限。儘管透過來自擁有基因匹配血親的骨髓捐贈,擁有超過90%的治癒率;但僅僅只有20%的患者有這樣的捐贈者。而其他藥物和支持性的治療大多只能緩解疾病,而無法徹底根治。
這種疾病是因為紅血球蛋白上的基因存在單一的鹼基突變,導致血紅蛋白的六個胺基酸位置上帶有纈氨酸而不是谷氨酸。這會將正常成人血紅素轉化為鐮狀血紅蛋白。當紅血球失去其攜帶的氧氣時,它會自行聚合,形成鏈狀結構,使細胞變形。
CRISPR/Cas9基因療法──Casgevy與Lyfgenia
簡單來說,CRISPR/Cas9就是一把「基因剪刀」,可以移除或植入目標基因來使細胞機制作用或沉默。在鐮刀型紅血球疾病中,扮演轉錄因子的重要蛋白名為BCL11A,負責控制Hbf基因的表現(存在時會關閉Hbf基因)。
Hbf,又稱為胎兒紅血球蛋白,是幫助嬰兒從母體血液接受氧氣的重要寫球蛋白。而編碼Hbf的基因會在胎兒出生六個月後左右被關閉,並轉變為HbA。
Casgevy便是利用剪斷BCL11A來使Hbf基因重新表現。對於接受治療的患者,科學家首先會抽取患者的骨髓幹細胞,並在實驗室中進行CRISPR基因編輯。同時,患者會接受化療以殺死骨髓幹細胞,來使基因編輯細胞不產生排斥。在植入基改完後的細胞後,超過93.5%的患者在為期12-24個月的追蹤下,沒有發生血管堵塞的情形。
另一項批准的基因療法被稱為Lyfgenia,它是透過將攜帶改良紅血蛋白基因的病毒載體植入患者體內,來阻止細胞發展為鐮刀狀型紅血球。而超過88%的患者在治療後的6-18個月內沒有出現血管阻塞情況。
資料來源:arstechnica
![]()


